 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
在1 000 K时,实验测得气相反应C2H5(g)→2CH3. 的速率常数表达式为k/s-1=2.0× ,设这时 。(1)试计
在1 000 K时,实验测得气相反应C2H5(g)→2CH3. 的速率常数表达式为k/s-1=2.0×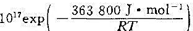 ,设这时
,设这时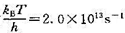 。(1)试计算反应的半衰期t1/2;(2)试计算C2H6(g)分解反应的活化熵
。(1)试计算反应的半衰期t1/2;(2)试计算C2H6(g)分解反应的活化熵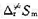 ;(3)已知1000 K时该反应的标准熵变
;(3)已知1000 K时该反应的标准熵变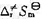 =74.1
=74.1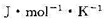 ,试将此值与(2)中所得的
,试将此值与(2)中所得的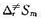 值比较,定性地讨论该反应的活化配合物的性质。
值比较,定性地讨论该反应的活化配合物的性质。
 答案
答案






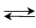 CH3COOH+CH3O 反应在25℃的平衡常数为0.22,乙酸甲酯和水的初始浓度分别为1.15mol/L和48.76mol/L。实验测得当反应进行到1h的时候,有34.92%的乙酸甲酯发生了水解。若正逆反应均为二级,试求反应速度常数k和k'。
CH3COOH+CH3O 反应在25℃的平衡常数为0.22,乙酸甲酯和水的初始浓度分别为1.15mol/L和48.76mol/L。实验测得当反应进行到1h的时候,有34.92%的乙酸甲酯发生了水解。若正逆反应均为二级,试求反应速度常数k和k'。 O2(g)可以进行完全,并设产物对反应速率无影响,经实验证明该反应是二级反应,速率方程可表示为
O2(g)可以进行完全,并设产物对反应速率无影响,经实验证明该反应是二级反应,速率方程可表示为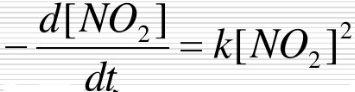
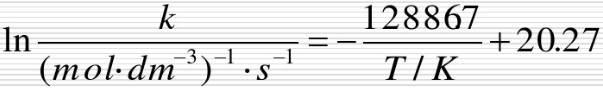

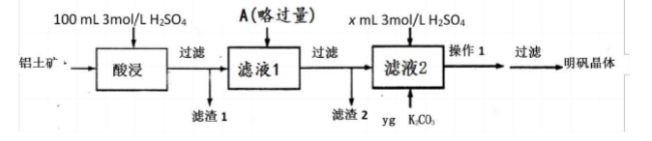 已知:二氧化硅不溶于水,也不与硫酸反应。
已知:二氧化硅不溶于水,也不与硫酸反应。 (6)工业生产中,获取明矾晶体后的母液应该()(填序号)。
(6)工业生产中,获取明矾晶体后的母液应该()(填序号)。



















