 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应HI(g)+CH3I(g)→CH4(g)+I2(g)在157℃时的速率常数k=l.7×10-5L·mol-1·s-1,在227℃时的速率常数k=4.0×10
已知反应HI(g)+CH3I(g)→CH4(g)+I2(g)在157℃时的速率常数k=l.7×10-5L·mol-1·s-1,在227℃时的速率常数k=4.0×10-3L·mol-1·s-1,求该反应的活化能。
 答案
答案
 请输入或粘贴题目内容
搜题
请输入或粘贴题目内容
搜题
 拍照、语音搜题,请扫码下载APP
拍照、语音搜题,请扫码下载APP
 题目内容
(请给出正确答案)
题目内容
(请给出正确答案)
已知反应HI(g)+CH3I(g)→CH4(g)+I2(g)在157℃时的速率常数k=l.7×10-5L·mol-1·s-1,在227℃时的速率常数k=4.0×10-3L·mol-1·s-1,求该反应的活化能。
 答案
答案
 更多“已知反应HI(g)+CH3I(g)→CH4(g)+I2(g)在157℃时的速率常数k=l.7×10-5L·mol-1·s-1,在227℃时的速率常数k=4.0×10”相关的问题
更多“已知反应HI(g)+CH3I(g)→CH4(g)+I2(g)在157℃时的速率常数k=l.7×10-5L·mol-1·s-1,在227℃时的速率常数k=4.0×10”相关的问题
第1题
A.50
B.0.01
C.10
D.无法确定
第2题
A.放出能量的反应
B.吸收能量的反应
C.氧化还原反应
D.可逆反应
第3题
A.挚痛chì胸膛táng喷涌而出yǒng誓言shì
B.仰望yáng呻吟yín端木蕻良gōng耻辱chǐrǔ
C.召唤zhào缠绕chán五彩斑斓lán场院cháng
D.山涧jiàn浆液jiāmg默契十足qiè污秽hiù
第5题
A.HI、I2、H2的浓度相等时
B.混合气体的颜色不变化时
C.混合气体的总压强不变化时
D.HI、I2、H2的反应速率之比为2:1:1时
第6题
A.239.2kJ
B.438.4kJ
C.119.6kJ
D.358.8kJ
第7题
A.等于5s
B.等于10s
C.大于10s
D.小于10s
第8题
HI(g)的分解反应在836K时其速率常数k=0.00105s-1,在943K时的速率常数k=0.00268s-1。试计算:
(1)该反应的活化能Ea;
(2)在773K时的速率常数k。
第9题
A.H2的消耗速率与HI的生成速率之比为2:1
B.若平衡正向移动,则V正一定增大
C.正、逆反应速率的比值是恒定的
D.达到平衡时,正、逆反应速率相等
第10题
已知基元反应CO(g)+NO2(g)=NO(g)+CO2(g),该反应的速率方程式为(),此速率方程为()定律的数学表达式,此反应对NO,是()级反应。总反应是()级反应
第11题
已知反应SnO2(s)+2H2(g)=Sn(s)+2H2O(g)和CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数分别为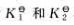 。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)
。则反应SnO2(s)+2CO(g)=2CO2(g)+Sn(s)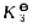 的=()。
的=()。